FDA de EEUU aprueba vacunas actualizadas contra COVID-19 para variantes en circulación
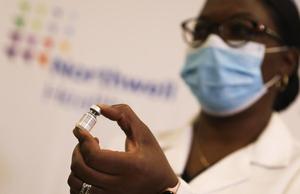
(201214) -- NUEVA YORK, 14 diciembre, 2020 (Xinhua) -- Una trabajadora de la salud muestra un frasco de la vacuna contra la COVID-19 en el Centro Médico Judío de Long Island, en Nueva York, Estados Unidos, el 14 de diciembre de 2020. Estados Unidos inició el lunes el despliegue de la primera vacuna contra la COVID-19 y las primeras dosis fueron administradas a los trabajadores de la salud y al personal de asilos. (Xinhua/Wang Ying) (ah) (ra) (vf)